免疫组化原理、步骤及应用
发布日期:2012-11-08 浏览次数:9983
免疫组化原理、步骤及应用
用标记的特异性抗体对组织切片或细胞标本中某些化学成分的分布和含量进行组织和细胞原位定性、定位或定量研究,这种技术称为免疫组织化学(immunohistochemistry,IHC)技术或免疫细胞化学(immunocytochemistry,ICC)技术。
根据抗原抗体反应和化学显色原理,组织切片或细胞标本中的抗原先和一抗结合,再利用一抗与标记生物素、荧光素等的二抗进行反应,前者再用标记辣根过氧化物酶(HRP)或碱性磷酸酶(AKP)等的抗生物素(如链霉亲和素等)结合,最后通过呈色反应或荧光来显示细胞或组织中化学成分,在光学显微镜或荧光显微镜下可清晰看见细胞内发生的抗原抗体反应产物,从而能够在细胞爬片或组织切片上原位确定某些化学成分的分布和含量。
 |
- 1、按标记物质的种类,如荧光染料、放射性同位素、酶(主要有辣根过氧化物酶和碱性磷酸酶)、铁蛋白、胶体金等,可分为免疫荧光法、放射免疫法、免疫酶标法和免疫金银法等。
- 2、按染色步骤可分为直接法(又称一步法)和间接法(二步、三步或多步法)。与直接法相比,间接法的灵敏度提高了许多。
- 3、按结合方式可分为抗原-抗体结合,如过氧化物酶-抗过氧化物酶(PAP)法;亲和连接,如卵白素-生物素-过氧化物酶复合物(ABC)法、链霉菌抗生物素蛋白-过氧化物酶连结(SP)法等,其中SP法是比较常用的方法;聚合物链接,如即用型二步法,此方法尤其适合于内源性生物素含量高的组织抗原检测。
- 1、免疫荧光方法
- 免疫荧光方法是最早建立的免疫组织化学技术。它利用抗原抗体特异性结合的原理,先将已知抗体标上荧光素,以此作为探针检查细胞或组织内的相应抗原,在荧光显微镜下观察。当抗原抗体复合物中的荧光素受激发光的照射后即会发出一定波长的荧光,从而可确定组织中某种抗原的定位,进而还可进行定量分析。由于免疫荧光技术特异性强、灵敏度高、快速简便,所以在临床病理诊断、检验中应用较广。
- 2、免疫酶标方法
- 免疫酶标方法是继免疫荧光后,60年代发展起来的技术。基本原理是先以酶标记的抗体与组织或细胞作用,然后加入酶的底物,生成有色的不溶性产物或具有一定电子密度的颗粒,通过光镜或电镜,对细胞表面和细胞内的各种抗原成分进行定位研究。免疫酶标技术是目前最常用的技术。该方法与免疫荧光技术相比的主要优点是:定位准确,对比度好,染色标本可长期保存,适合于光、电镜研究等。免疫酶标方法的发展非常迅速,已经衍生出了多种标记方法,且随着方法的不断改进和创新,其特异性和灵敏度都在不断提高,使用也越来越方便。目前在病理诊断中广为使用的有ABC法、SP三步法、即用型二步法检测系统等。
- 3、免疫胶体金技术
- 免疫胶体金技术是以胶体金金属颗粒作为标记物。胶体金是指金的水溶胶,它能迅速而稳定地吸附蛋白,对蛋白的生物学活性则没有明显的影响。因此,用胶体金标记一抗、二抗或其他能特异性结合免疫球蛋白的分子(如葡萄球菌A蛋白)等作为探针,就能对组织或细胞内的抗原进行定性、定位,甚至定量研究。由于胶体金有不同大小的颗粒,且胶体金的电子密度高,所以免疫胶体金技术特别适合于免疫电镜的单标记或多标记定位研究。由于胶体金本身呈淡至深红色,因此也适合进行光镜观察。如应用银加强的免疫金银法则更便于光镜观察。
- 1、特异性强。免疫学的基本原理决定抗原与抗体之间的结合具有高度特异性,因此,免疫组化从理论上讲也是组织细胞中抗原的特定显示,如角蛋白(keratin)显示上皮成分,LCA显示淋巴细胞成分。只有当组织细胞中存在交叉抗原时,才会出现交叉反应。
- 2、敏感性高。ABC法或SP三步法使抗体稀释上千倍、上万倍甚至上亿倍仍可在组织细胞中与抗原结合,这样高敏感性的抗体抗原反应,使免疫组化方法越来越方便地应用于常规病理诊断工作。
- 3、定位准确、形态与功能相结合。该技术通过抗原抗体反应及呈色反应,可在组织和细胞中进行抗原的准确定位,可同时对不同抗原在同一组织或细胞中进行定位观察,这样就可以进行形态与功能相结合的研究,对病理学领域开展深入研究是十分有意义的。
- 1、Western blotting:蛋白质免疫印迹,也是利用抗体抗原反应原理,结合化学发光等技术来检查组织或细胞样品内蛋白含量的检测方法。与免疫组化技术相比,定量可能更加准确;当然Western blotting也可定性和定位(通过提取膜蛋白或核蛋白、胞浆蛋白分别检测其中抗原含量,进而间接反映它们的定位),但敏感性远远低于免疫组化技术。
- 2、ELISA:酶联免疫吸附试验,也是利用抗体-抗原结合反应原理来检测体液或组织匀浆中蛋白含量。与免疫组化技术相比,定量最准确,是分泌性蛋白检测首选方法之一。
流程简介
- 1)石蜡切片,常规脱蜡至水。
- 2)0.3%或3%H2O2去离子水(无色液体)孵育10-30分钟,以灭活内源性过氧化物酶活性。
- 3)蒸馏水冲洗,PBS浸泡5分钟。
- 4)候选步骤:采用抗原修复:微波(建议30分钟内4次中火)、高压、酶修复方法。自然冷却。
- 5)血清封闭:室温15-30分钟,尽可能与二抗来源一致。倾去,勿洗。
- 6)滴加适当比例稀释的一抗,37℃孵育2~3小时或4℃过夜(最好复温)。PBS冲洗,3分钟×5次。
- 7)滴加生物素标记的二抗,室温或37℃孵育30分钟-1h。
- 8)PBS冲洗,3分钟×5次。
- 9)滴加SP(链霉亲和素-过氧化物酶),室温或37℃孵育30分钟-1h。
- 10)PBS冲洗,3分钟×5次。
- 11)显色剂显色(DAB等)。
- 12)自来水充分冲洗。
- 13)可进行复染,脱水,透明。
- 14)选择适当的封片剂封片。
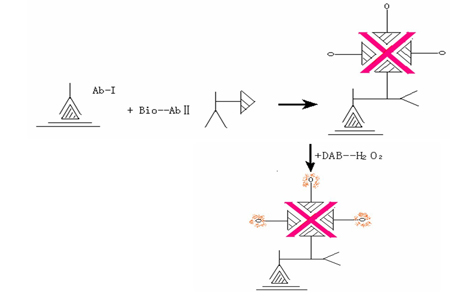 |
| 免疫组化ABC法 |
- 1) 4%多聚甲醛常规灌注固定,取材并置20%蔗糖溶液(4℃)过夜,蜡块制作,切片,贴片。0.01M PBS清洗5min×3次;
- 2) 脱蜡、水化:用二甲苯两次10min,用梯度乙醇由低浓度到高浓度进行水化;
- 3) 加入0.3%的过氧化氢甲醇溶液(甲醇80ml+0.01M PBS 100ml+30%过氧化氢)30min,以消除内源性过氧化物酶的影响,0.01M PBS清洗5min×3次;
- 4) 加入0.3% Triton X-100(0.3ml Triton X-100+0.01 M PBS 100ml)30min,以增加细胞的通透性,0.01M PBS清洗5min×3次;
- 5) 加入用血清稀释液(牛血清白蛋白1.00g+0.01M PBS 100ml+叠氮纳0.08g)稀释的一抗,4℃过夜。吸去抗体,0.01M PBS洗5min×3次;
- 6) 加入0.01M PBS稀释的的二抗,室温孵育2h。0.01M PBS洗5min×3次;
- 7) 加入ABC复合物之类的抗体,室温孵育2h,0.01M PBS洗5min×3次;蒸馏水迅速冲三次;
- 8) 加入显色液,进行免疫组织化学显色,时间一般3~10min,可不时在显微镜下进行观察,待细胞着色而背底颜色较淡时马上吸去显色液,用蒸馏水迅速冲三次后加入0.01M PBS终止反应;
- 9) 苏木素复染;
- 10) 梯度酒精脱水之后,透明,封片,拍照。
- 1、应用于肿瘤分期
- 免疫组化通过显示基底膜缺无或明显断裂来确定有微浸润肿瘤的早期,还可以检测骨髓及淋巴结隐匿性转移癌。
- 2、检测肿瘤相关抗原:甲胎蛋白(AFP、甲状腺球蛋白(Tg))等
- 3、检测肿瘤细胞增生标志物
- 目前被广泛采用的两种增殖相关标志物是Ki-67及PCNA(增埴细胞核抗原)。Ki-67与PCNA免疫反应性与细胞增生的形态学特征关系密切,特别是与有丝分裂数及肿瘤分级相关。在乳腺癌、前列腺癌、结肠癌、肺癌、肝癌、胃癌和一些淋巴瘤及肉瘤,采用Ki-67与PCNA免疫组化分析,均显示有增殖证据,提示这些肿瘤病人更容易进展。高Ki-67及PCNA标记指数病人无病生存率及总生存率明显下降。
- 4、检测癌基因产物和抑癌基因产物:c-erbB-2、表皮生长因子受体(EGFR)、P53等
- 5、预测治疗反应
- 例如,免疫组化可预测乳腺癌对激素治疗的反应性。无ER或PR表达的肿瘤对激素治疗通常反应性差,而ER及PR阳性肿瘤则对激素治疗反应性高。
- 6、应用于临床病理诊断
- 许多肿瘤组织细胞在显微镜下看起来非常相似,以致于病理医生难以完全准确地判断出肿瘤的性质。使用免疫组化检测肿瘤细胞的表面和细胞内特异性的物质表达,有助于明确肿瘤的性质和组织来源。
【上一篇】western blot原理及步骤
【下一篇】BD PMG协助发现调控T细胞分化增殖的关键因素


